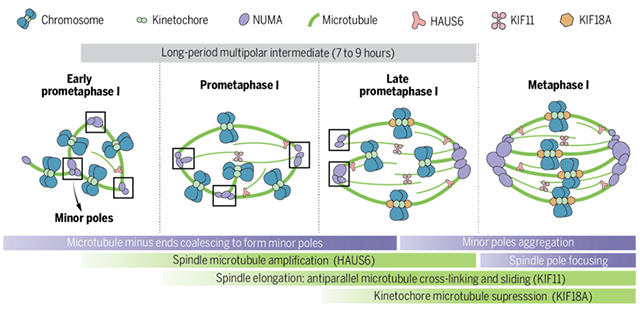
图 人类卵母细胞双极纺锤体组装机制
在国家自然科学基金项目(批准号:32130029、82271685、82325021、82101737、82171643、82288102)等资助下,复旦大学王磊教授、桑庆研究员及上海交通大学附属国际和平妇幼保健院李文主任医师在人类卵母细胞纺锤体双极化机制方面取得进展,研究成果以“人类卵母细胞纺锤体双极化机制(Mechanisms of minor pole–mediated spindle bipolarization in human oocytes)”为题,于2024年8月23日在《科学》(Science)杂志上在线发表。论文链接:https://www.science.org/doi/10.1126/science.ado1022。
纺锤体组装是决定染色体精确分离的重要前提,是有丝分裂/减数分裂的关键事件之一。纺锤体组装过程主要包括纺锤体微管聚合以及纺锤体双极化(spindle bipolarization)。纺锤体微管聚合启动后,伴随一系列形态变化,最终形成双极状纺锤体,这一过程被称为纺锤体双极化。双极化异常会导致纺锤体组装失败、破坏有丝分裂/减数分裂、引起细胞/卵子发育异常。然而,人类卵母细胞中纺锤体双极化的过程及机制仍不清楚。
该研究通过对1800多个人类卵母细胞进行高分辨成像技术发现人类卵母细胞纺锤体微管聚合启动后,会经历一段较长时间的 “多极纺锤体”(Multipolar spindle)阶段,而后才形成双极状纺锤体。人类卵母细胞多极纺锤体状态持续时间长达7-9个小时,呈现出与有丝分裂及其他哺乳动物卵母细胞的纺锤体双极化过程截然不同的形态变化,揭示人类卵母细胞纺锤体组装的独特机制。进一步发现调控纺锤体双极化的关键蛋白HAUS6、KIF11和KIF18A在此过程中发挥重要作用。并且在临床生殖障碍性疾病患者中鉴定到编码上述关键蛋白的基因存在突变,这些突变位点会引起不同程度的纺锤体双极化异常,从而导致卵母细胞成熟障碍、受精失败及早期胚胎发育停滞。
该研究揭示了人类卵母细胞纺锤体双极化的独特病理生理机制(图),发现“多极纺锤体”是人类卵母细胞纺锤体双极化过程中必经的生理状态,明确了调控此过程的关键蛋白;揭示关键基因突变导致双极化异常引起卵子和胚胎发育障碍的病理机制。该研究为人类卵母细胞纺锤体组装过程提供了新的认识,并将为临床生殖障碍疾病的诊疗提供科学依据。